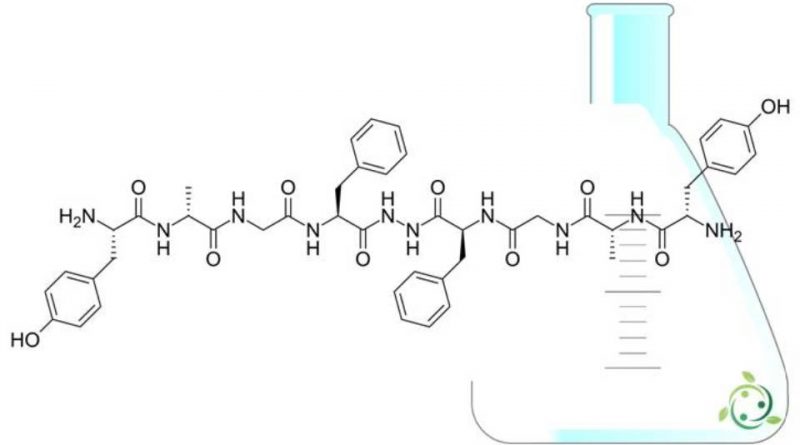
Bifalina
Bifalina
La bifalina è un peptide oppioide dimerico (Tyr-D-Ala-Gly-Phe-NH)2, costituito da due identici tetrapeptidi correlati alle encefaline e connessi da coda a coda attraverso un ponte idrazinico.
Nella nomenclatura ufficiale IUPAC, la bifalina prende il seguente termine: (2S,2’S)-N,N’-[(2R,8S,13S,19R)-8,13-Dibenzil-3,6,9,12,15,18-esaosso-4,7,10,11,14,17-esaazaicosano-2,19-dil]bis[2-ammino-3-(4-idrossifenil)propanammide].
La bifalina ha formula bruta o molecolare: C46H56N10O10.
Nella bifalina la presenza di due distinti farmacofori conferisce a questa molecola una elevata affinità sia per i recettori oppioidi μ che per i δ (con una EC50 per i due recettori di circa 1-5 nM), mostrando quindi un’attività analgesica.
La bifalina, inoltre, manifesta un profilo antiniocicettivo degno di considerazione.
Somministrando nei topi, per via intracerebroventricolare, la bifalina, questa mostra una capacità 7 volte maggiore del potente agonista oppioide etorfina e 7000 volte più alta della morfina; da sottolineare, inoltre, che bifalina e morfina si sono mostrate equipotenti in seguito a somministrazione interperitoneale.
Per di più l’efficiente capacità di questa molecola, in vivo, è accompagnata da ridotti effetti collaterali, soprattutto per quanto attiene alla comparsa di dipendenza in seguito all’assunzione prolungata.
È per questo che sono state compiute molti studi al fine di ottenere maggiori informazioni sulle relazioni struttura attività (SAR).
I risultati ottenuti hanno portato a considerare che, almeno per il legame al recettore μ, la presenza di due farmacofori non è necessaria.
Si sottolinea come la Tyr1 sia indispensabile per l’attività analgesica, mentre la sostituzione della Phe in 4 e 4′ con amminoacidi non aromatici ma lipofili non influenza particolarmente l’affinità recettoriale; in generale la posizione 4,4′ è considerata importante per la realizzazione di analoghi dotati di maggiore potenza e per modulare la selettività δ/μ. Il linker idrazinico non è fondamentale per l’attività e l’affinità, e può essere convenientemente sostituito con vari sostituenti cicloalifatici dotati di maggiore rigidità conformazionale.
Avvertenza: le informazioni riportate non sono consigli medici e potrebbero non essere accurate. I contenuti hanno solo fine illustrativo e non sostituiscono il parere medico.